적 요본 연구는 전국에 분포하는 조릿대[Sasa borealis (Hack.) Makino & Shibata]의 12 개체군을 대상으로 유전다양성을 분석하고, 이러한 분석 결과를 식물지리학적인 해석을 통하여 기후변화와 같은 변화 요인을 객관적으로 측정하고 예측할 수 있는 방법을 제시하기 위해 수행되었다. AFLP (amplified fragment length polymorphism) 분석을 통한 유전다양성 조사 결과, 조릿대 개체군의 유전다양성(PPL = 37.2%, h = 0.143, I = 0.205)과 유전적 분화도(Gst = 0.324, θB = 0.395)는 비교적 높은 수준으로 나타났다. AMOVA (Analysis of molecular variance) 분석 결과에서도 전체 유전적 변이 중 47.7%가 개체군 간 변이에 의한 것으로 나타났다. 그리고 조릿대 개체군들의 유전다양성은 위도가 높아짐 따라 감소하는 것이 확인 되었으며, 이는 남방계 식물인 조릿대의 분포가 낮은 위도에서 높은 위도로 전파된 과정과 일치하는 것으로 해석할 수 있다. 따라서 식물 개체군의 AFLP 분석 결과를 위도 변화와 비교 분석함으로써 기후변화에 따른 분포 변화의 정도를 파악하고 주요 식물의 보전 전략을 세우는 데 필요한 정보를 제공할 수 있다.
Abstract
Sasa borealis (Hack.) Makino & Shibata is widely distributed in South Korea. With amplified fragment length polymorphism (AFLP) markers, we analyzed the genetic diversity of S. borealis to predict and measure the phytogeographical factors of these populations. Relatively high levels of genetic diversity (PPL = 37.2%, h = 0.143, I = 0.205) and genetic differentiation (Gst = 0.324, θB = 0.395) were confirmed in populations of S. borealis. Moreover, an analysis of molecular variance (AMOVA) showed that the rate of differentiation among the populations was 47.7%. The results showed that genetic diversity is inversely proportional to the latitude of the S. borealis populations, indicating that the distribution of S. borealis may have extended from lower to higher latitudes. This method of investigating the correlation between genetic diversity and latitude presents critical information for estimating changes in distributions and plant conservation due to climate change.
조릿대[Sasa borealis (Hack.) Makino & Shibata]는 벼과(Poaceae Barnhart)의 대나무아과(Bambusoideae Luerss.)에 속하는 온대 목본성 대나무(temperate woody bamboo)이다. 전세계에 약 60종이 분포하고 있으며, 이 중 대부분은 아시아에 생육한다(Clayton and Renvoize, 1986; Zhang and Clark, 2000). 한반도의 조릿대속에는 지금까지 총 5종 1변종이 보고되어 있다; 조릿대[Sasa borealis (Hack.) Makino & Shibata], 섬조릿대[S. kurilensis (Rupr.) Makino & Shibata], 섬대[S. borealis var. gracilis (Nakai) T.B.Lee], 제주조릿대(S. quelpaertensis Nakai), 갓대[S. chiisanensis (Nakai) Y.N.Lee], 신이대(S. coreana Nakai) (Nakai, 1952; Lee, 2003; Lee, 2006). 대나무아과는 상록성으로 남방계 식물이라고 할 수 있으며, 우리나라 북방한계선은 서해에서는 백령도, 서부 내륙지역은 용문산-명지산, 그리고 동해안은 추애산-명천에 이르는 것으로 보고된 바 있다(Kong, 1985; 2001). 그러나 이는 주로 문헌 조사와 단순한 분포 조사를 통하여 파악한 자료에 근거한 것이다. 조릿대는 한반도 전역 산지와 일본에 주로 분포하며 북쪽으로는 북해도, 남쪽으론 규슈 지방까지 분포하는 것으로 알려져 있다(Tsuyama et al., 2011).
위도에 따른 생물다양성에 대한 연구는 위도가 올라갈수록 생물다양성이 감소하는 것으로 알려져 있고(Fischer, 1960), 또한 생물다양성과 함께 유전 다양성도 위도가 높아짐에 따라 감소하는 것을 보여준다(Martin and McKay, 2004; Falahati-Anbaran et al., 2007). 이렇게 위도가 높아질수록 유전다양성이 낮아지는 것은 계절적 변이와 일조량의 감소, 그리고 빙하의 증가에 의한 지형 변화 등의 영향이 큰 것으로 생각되고 있다(Martin and McKay, 2004). 위도와 유전적 다양성의 관계는 식물과 동물에서 확인되고 있다. 즉, 동위효소를 사용한 대마황(Casuarina cunninghamiana)에 대한 연구와 microsatellite를 이용한 집참새[house sparrow (Passer domesticus)]의 유전적 다양성 분석 결과에서 위도와 유전적 다양성은 상관관계를 나타내는 것으로 알려졌다(Moran et al., 1989; Schrey et al., 2011).
Amplified fragment length polymorphism (AFLP) 마커는 개체군 보전 연구 그리고 개체군 구조와 유전적 다양성 분석 다양한 연구에 이용되었으며 해상력이 높기 때문에 개체군의 유전적 특성을 잘 반영하는 것으로 알려져 있다(Kim et al., 2011, 2012; Jung et al., 2014). 조릿대가 포함된 대나무아과는 AFLP, inter-simple sequence repeats (ISSR), random amplified polymorphic DNA (RAPD) 와 같은 다양한 마커를 이용한 유전적 다양성 분석이 이루어졌다(Hsiao and Lee, 1999; Suyama et al., 2000; Tian et al., 2012).
조릿대는 남방계 식물로 이미 알려져 있고 국내 산지에 폭넓게 분포(Kong, 1985; 2001)하고 있는 분류군이므로 기후변화와 같은 환경 요인에 의한 식물지리학적 변이 분석에 적합한 분류군으로 선택되었다. 본 연구에서는 AFLP 마커를 이용하여 우리나라에 전역에 분포하고 있는 조릿대 개체군들의 유전적 다양성을 분석하였으며, 위도에 따른 유전적 다양성의 변이 양상 및 개체군의 유전적 분화도를 비교하였다. 이와 같은 위도에 따른 조릿대 개체군들의 유전적 변이를 식물지리학적인 해석을 통하여 기후변화와 같은 환경 요인을 객관적으로 측정하고 예측할 수 있는 방법을 제공하고자 하였다.
재료 및 방법재료시료의 채취는 개체군내 개체간의 거리를 최소 10 m 이상으로 유지하면서 진행되었다. 시료는 전라남도 완도군, 두륜산, 지리산과 강원도 태백산, 설악산, 석병산, 계방산 그리고 경상북도 상운산, 문경시와 경기도 칠현산 등 12개 지역에서 채집하였다(Fig. 1). 전체 72개체가 유전다양성 분석에 사용되었으며, 각 개체군별로 채집된 개체수는 Table 1과 같다.
본 연구에서는 울릉도의 섬조릿대[Sasa kurilensis(Rupr.) Makino and Shibata]와 제주도의 제주조릿대(S. quelpaertensis Nakai)를 포함한 분류군들로 부터 얻은 AFLP 분석 자료를 토대로 neighbor-joining 수지도를 작성한 후 여기에서 하나의 독립된 클러스터를 보이는 조릿대(Sasa borealis) 개체군들만을 시료로 사용하였다. 개체군을 대표하는 개체를 대상으로 확증표본을 제작 하였으며, 이들은 아주대 생명과학과 식물표본실(AJOU)에 보관되어 있다.
DNA 추출 및 AFLP 분석채집된 식물체의 잎은 70% 에탄올로 세척 후 실리카 겔로 건조하여 DNA 추출에 사용하였다. DNA 추출법은 Dolye and Doyle (1987)에 기초한 CTAB 방법(Chen and Ronald, 1999; Kim et al., 2011)을 사용하였다. 추출된 DNA는 자외선 분광기(Genova, Genway, UK)에서 260 nm와 280 nm 파장에서 흡광도를 측정하여 정량하였으며, 정량된 DNA는 100 ng/μL 농도로 희석하여 사용하였다. AFLP 분석은 5개체군에서 8개체를 선별하여 12개의 AFLP 프라이머 조합을 통해 분석한 결과 상대적으로 높은 변이를 보이는 4개 조합을 사용하였다(Table 2). AFLP 분석은 Vos et al. (1995)의 방법을 변형한 형광표지된 프라이머를 사용하여 분석을 수행하였다(Kim et al., 2008). AFLP 결과 나온 밴드는 존재하면 ‘1’로 부재하면 ‘0’로 코딩되었으며, 모든 개체가 가지는 단형성의 밴드와 5% 미만의 빈도를 보이는 다형성 밴드는 분석에서 제외하였다(Keiper and McConchie, 2000).
자료분석유전적 다양성을 추정하기 위해 POPGENE 1.31 (Yeh et al., 1997)을 이용하여 다형성 유전자위의 백분율(PPL, percentage of polymorphic loci), Nei (1973; 1978)의 이형접합도(h), Shannon and Weaver’s index (I)를 구하였으며, 개체군간의 유전적 분화도(GST), 개체군간의 유전자 흐름(Nem)을 계산하였다. 베이스 추론을 사용하는 Hickory 1.1을 이용해 개체군 분화도(θB)를 결정하였다(Holsinger and Lewis, 2005). Deviance information criterion (DIC) 값을 사용해 세 가지 모델(Full model, f = 0 model, f -free model) 중 안정적인 값을 얻었다. 유전적 구조의 평가에는 Arlequin 3.5에 내장된 AMOVA (Analysis of Molecular Variance)를 사용하였다(Excoffier et al., 1992; Excoffier and Lischer, 2010). 위도와 개체군 다양성 사이의 상관관계를 보여주는 산점도와 선형회귀분석은 Sigma Plot 10.0 (Systat, San Jose, CA, USA)을 사용하였다. 개체군 간의 유전적 유연관계를 파악하기 위한 neighbor-joining 수지도는 유전적거리(Pairwise Φst)를 기초하여 MEGA 5 프로그램을 통해 작성되었다(Tamura et al., 2011). 유전적 거리와 지리적 거리의 상관관계를 보여주는 Mantel test는 TFPGA 1.3 (Miller, 1997)을 이용하여 수행하였다(Mantel, 1967; Kim et al., 2011).
결 과AFLP 유전다양성조릿대 개체군의 4개의 AFLP 프라이머 조합을 통한 유전다양성 분석에서 총 184개의 밴드를 확인하였으며, 이 중 122개(66.3%)의 밴드는 다형성을 보여주었다(Table 2).
조릿대 개체군의 유전다양성의 평균값은 PPL = 37.2%, h = 0.143, 그리고 I = 0.205으로 분석되었다(Table 3). 개체군 내 유전다양성은 지리산 개체군(JBJ)에서 가장 높은 변이(PPL = 80.3%; h = 0.269; I = 0.406)를 보여주었으며, 칠현산 개체군(GGC)에서 가장 낮은 변이(PPL = 8.2%; h = 0.032; I = 0.047)를 보여주었다(Table 3). 전라도의 개체군들(JNS, JND)의 유전다양성(PPL)은 40% 이상의 변이를 나타내었다. 경상도의 개체군들(GBS, GBM)도 마찬가지로 40% 이상의 변이를 보여주었다. 강원도 개체군들(GWT, GWY, GWS, GWB, GWG)은 20% - 35%의 다양성을 보여주며, 경기도 개체군(GGC)은 약 10%의 다양성을 나타내었다(Table 3).
각 개체군의 유전적 분화 및 특성베이스 접근(Bayesian approach)에 의한 개체군 간 유전적 분화도(θB)를 세 가지 모델에 따라 분석한 결과 가장 낮은 DIC값을 보이는 full model이 선택되었다. 분화도 값은 0.395로 나타났다. 이 값은 유전적 분화도의 다른 접근인 Nei (1973)에 의한 유전적 분화도(GST = 0.324)와 유사한 수준이다. 개체군 간 유전자 흐름(Nem)은 GST 값을 통해 계산되었으며 0.671로 나타났다. 조릿대 개체군을 두 개의 계층으로 구분하여 AMOVA 분석 결과 유전 변이 전체 중 47.7%가 개체군 간의 차이에서 나타났으며 나머지 52.3%는 개체군 내 개체간의 차이에서 기인한 것으로 나타났다.
개체군 간의 유전적 거리(pairwise Φ st)를 구한 결과 전라남도의 두륜산(JND)과 완도 상황봉(JNS) 개체군이 0.059로 최소값을 보였다. 경기도의 칠현산(GGC)과 강원도 설악산(GWS) 개체군 간의 유전적 거리는 0.733으로 최대값을 나타냈다. Mantel test 결과 개체군간 유전적 거리와 지리적 거리 간에는 유의하지 않은 상관관계(r = 0.378, P = 0.006)를 보이는 것으로 나타났다(Fig. 3). 유전적 거리를 이용한 개체군간의 neighbor-joining 수지도를 작성한 결과 강원도의 다섯 개체군(GWT, GWY, GWS, GWB, GWG)과 경상북도 상운산 개체군(GBS)이 하나로 유집되었으며, 경기도 칠현산(GGC), 충청북도 속리산(CBS), 전라북도 지리산(JBJ)의 개체군들과 경상북도 문경 개체군(GBM)이 하나로 유집되었다. 또 전라남도 완도의 상황봉 개체군(JNS)은 해남의 두륜산 개체군(JND)과 유집이 되었다(Fig. 4).
고 찰유전다양성생물들의 유전적 다양성은 지리적인 분포, 개체군의 유전적 구조와 상관관계를 보이는 것으로 잘 알려져 있다(Fisher, 1960). 즉, 분포 범위가 좁거나, 천이의 초기-중기단계 그리고 유전적 부동의 결과는 낮은 유전적 다양성을 초래하며, 분포 범위가 광범위 할 경우, 천이의 후기단계 그리고 유전적 부동이 적을 때 높은 유전적 다양성을 나타낸다(Loveless and Hamrick, 1984). 조릿대 개체군에서 관찰된 유전다양성의 평균(PPL = 37.2%; h = 0.143)은 대나무아과의 근연속인 해장죽속(Arundinaria)과 비교할 경우 높은 것으로 나타났다. 즉, 북미의 온대지역에 분포하는 Aundinaria gigantea (h = 0.055)나 A. appalachiana (h = 0.052), 그리고, A. tecta (h = 0.054)보다 높은 것으로 나타났다(Triplett et al., 2010). 조릿대는 같은 속에서 국내에 가장 광범위하게 분포하고 있으며, 개체군이 크고, 유전적 부동 효과가 거의 없기 때문에 상대적으로 높은 유전 다양성을 유지하고 있는 것으로 생각된다.
조릿대 개체군들의 유전다양성은 분포 지역에 따라 비교적 넓은 범위의 변이를 나타낸다(PPL = 8.2% - 80.3%; h = 0.032 - 0.269). 개체군간에서 낮은 유전다양성 값을 보이는 근연속의 Arundinaria gigantea (h = 0.055), A. appalachiana (h = 0.052), A. tecta (h = 0.054) 와 비교하면 경기도 칠현산(GGC)은 보다 낮은 값(h = 0.032)을 가진다(Triplett et al., 2010; Table 3). 경기도 지역의 개체군(GGC)과 강원도 지역의 개체군들(GWT, GWY, GWS, GWB, GWG)이 평균(h = 0.143)보다 낮은 유전다양성을 보여주고 있는 것은 조사된 조릿대 개체군 중에서 가장 북쪽에 분포하고 있는 개체군들의 창시자효과로 상대적으로 천이의 초기단계에 있는 것으로 추정된다(Loveless and Hamrick, 1984; Nakajima et al., 1991). 반면 조릿대의 평균 유전다양성 보다 높은 유전다양성을 갖는 전라도(JND, JNS, JBJ)와 경상도(GBS, GBM)의 조릿대 개체군은 상대적으로 천이의 후기단계로 생각할 수 있다(Loveless and Hamrick, 1984).
유전적 분화 및 유연관계개체군 간 유전적 분화는 개체군의 생활사와 교배방법 등에 영향을 받는다(Loveless and Hamrick, 1984). 일년생 식물 종(GST= 0.430)은 다년생 식물 종(GST= 0.077~0.262)보다 높은 유전적 분화도를 보인다. 자가수분을 선호하는 식물 종(GST= 0.523)은 타가수분을 선호하는 식물 종(GST= 0.118)보다 높은 유전적 분화도를 보이며 자가수분과 타가수분을 함께하는 식물 종(GST= 0.243)은 중간 값을 갖는다(Loveless and Hamrick, 1984). 조릿대 개체군 간 유전적 분화도(GST= 0.324, θB= 0.395)는 다년생 식물 종 보다 높은 유전적 분화도 값을 가지며, 자가수분과 타가수분을 함께하는 식물 종과 유사한 값을 갖는다. AMOVA분석에 의한 개체군 내 개체간의 변이는 52.3%로 보였으며, 47.7%는 개체군 간의 차이로 나타났다(Table 5). 조릿대의 개체군간의 유전적 분화가 높은 이유는 개체군간의 유전자 이동이 적기 때문으로 해석할 수 있다. 이번 연구에서 분석된 조릿대 개체군간의 유전자 흐름(Nem = 0.671)은 낮은 값으로 이러한 해석을 지지해준다. Neighbor-joining 방법에 의한 개체군간의 유전적 유연관계를 분석한 결과 강원도의 다섯 개체군(GWT, GWY, GWS, GWB, GWG)과 경상북도 상운산 개체군(GBS)이 하나로 유집되었으며, 경기도 개체군(GGC), 충청북도 개체군(CBS), 지리산 개체군(JBJ)과 경상북도 문경 개체군(GBM)이 하나의 그룹을 형성하였다. 그리고 전라남도 상황봉 개체군(JNS)과 두륜산 개체군(JND)이 함께 유집되었다(Fig. 4). 상황봉과 두륜산을 제외한 다른 개체군들의 지리적 위치는 남-북으로 길게 분포되어 있으며(Fig. 1), 그룹 내에서의 유전적 유연관계가 상대적으로 가깝다(Fig. 4). 이번에 조사된 조릿대 개체군들 중에서 지리적으로 가깝지만 유전적으로는 거리가 먼 개체군들이 존재한다. 개체군의 지리적 분포와 유전적 유연관계를 나타내는 Mantel test 결과, 다소 낮은 상관관계(r = 378, P = 0.006)를 보이는 것은 이러한 개체군들의 유전적 특성과 거리와의 관계에 기인하는 것으로 보인다.
조릿대의 분포와 식물지리학적 이동 양상유전다양성이 기원에서 멀어질수록 감소한다는 것은 잘 알려져 있다(Hamrick et al., 1992). 본 연구에서 조릿대 개체군의 유전다양성은 위도가 증가함에 따라 감소하며, 이에 따른 유의한 상관관계(PPL, r = 0.731, P = 0.007; h, r = 0.719, P = 0.009; I, r = 0.743, P = 0.006)를 보여준다(Fig. 2). 이런 결과는 남방계 식물인 조릿대가 낮은 위도에서부터 높은 위도로 분포가 확장되어 지고 있다고 해석할 수 있다. 전라도와 경상도 개체군들은 평균보다 높은 유전다양성 값을 보여 주고 있고, 이에 비하여 북쪽에 있는 경기도와 강원도 개체군들은 상대적으로 낮은 유전다양성 값을 가지고 있는 것으로 나타났다(Table 3). 앞으로 전세계적인 기후변화에 의하여 조릿대의 분포가 북쪽으로 보다 확장될 경우에 현재 낮은 다양성을 갖는 중부지방 개체군들의 유전다양성은 북쪽에 위치한 개체군들 보다 상대적으로 높아지게 될 것이라고 예측할 수 있다.
국내의 식물구계 구분은 주로 식물의 분포와 기후대의 양상에 따라 결정되는 것으로 보고되었다(Yim and Kira, 1977; Lee and Yim, 1978). 본 연구 결과 개체군의 AFLP 분석을 통한 유전다양성의 위도에 따른 분석은 기후변화에 따른 식물들의 분포지 변화 예측과 주요 식물들의 보전 전략을 세우는 데 주요한 정보를 제공할 수 있을 것으로 생각된다. 이와 함께 중국, 일본, 대만 등지에 분포하는 근연종과 근연속을 포함한 계통분석과 haplotype 분석을 추가하게 된다면 조릿대속 전체의 동아시아적 식물지리학적 역사를 가늠할 수 있을 것이다.
ACKNOWLEDGMENTS본 연구는 두 번째 저자인 유다솜의 석사학위 청구 논문의 일부로 진행이 되었다. 유전다양성 분석에 유익한 조언을 하여 준 가천대학교의 김창균박사와 야외 채집과 자료정리에 많은 도움을 준 아주대학교 식물계통분류학 연구실의 류영일과 강동윤에게 고마운 마음을 전한다. 또한 본 논문의 원고를 심사하여 준 익명의 두 심사자에게도 감사드린다. 그리고, 본 연구는 한국연구재단 일반연구자지원사업(NRF-2013R1A1A2011078)의 지원으로 수행되었다.
Fig. 1.Location of 12 populations of Sasa borealis in South Korea. Abbreviations are same as in Table 1. 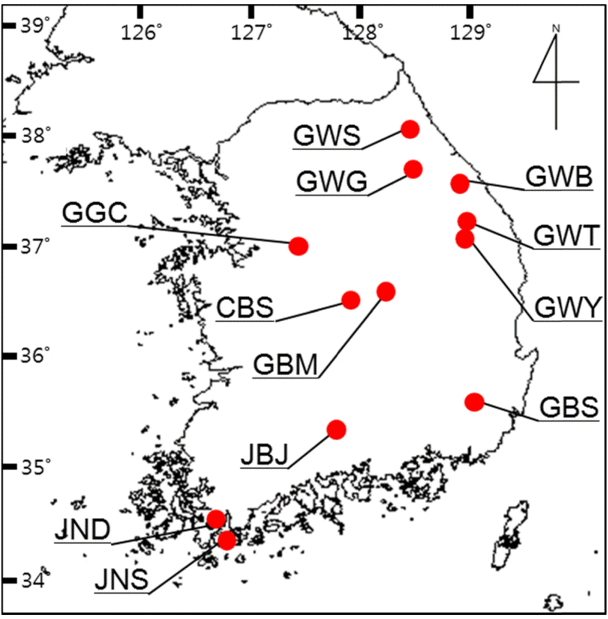
Fig. 2.Correlation between genetic diversity and latitude of Sasa borealis populations. A, Scatter diagram of percentage of polymorphic loci (PPL) against latitude; B, Scatter diagram of Nei’s unbiased expected heterozygosity (h) against latitude; C, Scatter diagram of Shannon index (I) against latitude. 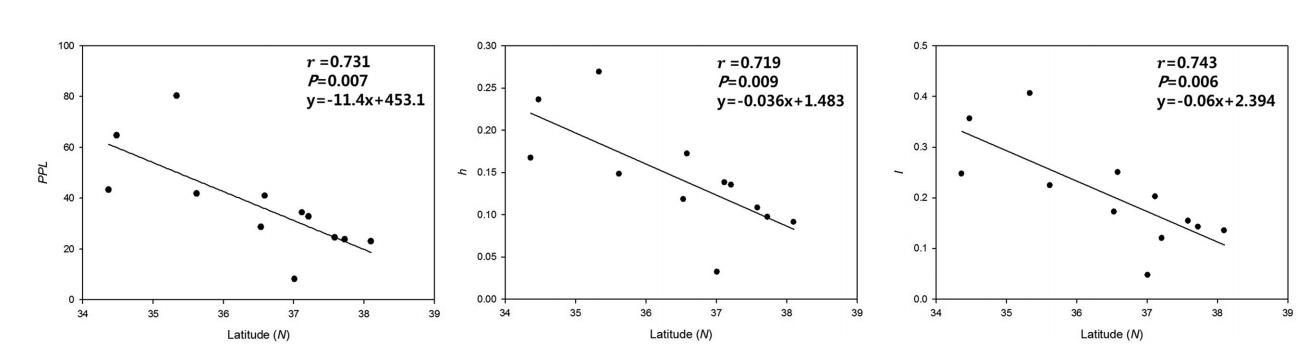
Fig. 3.Scatterplot and correlation between genetic distances (pairwise Φ st) and geographical distances based on amplified fragment length polymorphism (AFLP) markers of Sasa borealis populations (r = 0.378, P = 0.006). 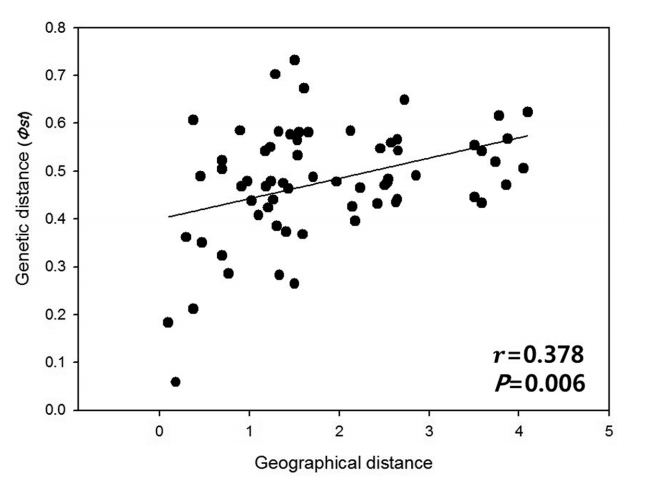
Fig. 4.Neighbor-joining dendrogram of Sasa borealis populations based on genetic distance (pairwise Φst) using amplified fragment length polymorphism (AFLP) markers. Abbreviations are same as in Table 1. 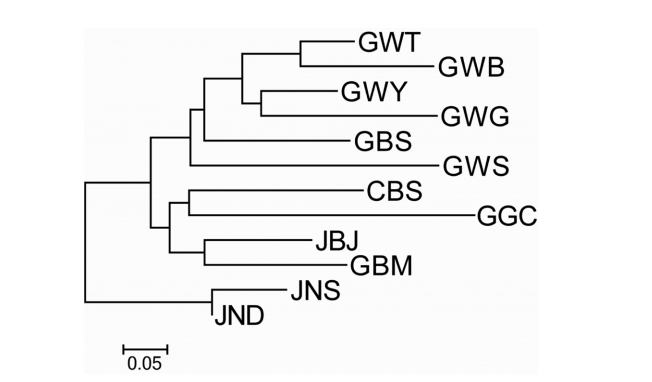
Table 1.Geographic information and sample size of Sasa borealis populations in Korea. Table 2.Polymorphic bands generated by amplified fragment length polymorphism (AFLP) primer combinations in 12 populations of Sasa borealis. Table 3.Genetic diversity based on amplified fragment length polymorphism (AFLP) markers within 12 populations of Sasa borealis. Abbreviations are same as in Table 1. PPL, percentage of polymorphic loci; h, Nei’s (1978) unbiased expected heterozygosity; I, Shannon and Weaver’s (1949) index. Table 4.Genetic differentiation (θ B) calculated with three different models by using the Bayesian approach.
Table 5.Summary of the analysis of molecular variance (AMOVA) within/among 12 populations based on amplified fragment length polymorphism (AFLP) markers.
Literature CitedChen, DH and Ronald, PC. 1999. A rapid DNA minipreparation method suitable for AFLP and other PCR applications. Plant Molecular Biology Reporter 17: 53-57.
Clayton, WD and Renvoize, SA. 1986. Genera graminum: grasses of the World. Royal Botanic Gardens, Kew, Paris.
Doyle, JJ and Doyle, JL. 1987. A rapid DNA isolation procedure for small quantities of fresh leaf tissue. Phytochemical Bulletin 19: 11-15.
Excoffier, L and Lischer, HE. 2010. Arlequin suite ver. 3.5: a new series of programs to perform population genetics analyses under Linux and Windows. Molecular Ecology Resources 10: 564-567.
Excoffier, L. Smouse, PE and Quattro, JM. 1992. Analysis of molecular variance inferred from metric distances among DNA haplotypes: application to human mitochondrial DNA restriction data. Genetics 131: 479-491.
Falahati-Anbaran, M. Habashi, AA. Esfahany, M. Mohammad, SA and Ghareyazie, B. 2007. Population genetic structure based on SSR markers in alfalfa (Medicago sativa L.) from various regions contiguous to the centers of origin of the species. Indian Academy of Science 86: 59-63.
Fischer, AG. 1960. Latitudinal variations in organic diversity. Society for the Study of Evolution 14: 64-81.
Hamrick, Jl. Godt, MJW and Sherman-Broyles, SL. 1992. Factors influencing levels of genetic diversity in woody plant species. Forestry Sciences 42: 95-124.
Holsinger, KE and Lewis, PO. 2005. A package for analysis of population genetic data, ver. 1.0.4, Department of ecology and evolutionary biology, University of Connecticut, Storrs, CT.
Hsiao, JY and Lee, SM. 1999. Genetic diversity and microgeographic differentiation of Yushan cane (Yushania niitakayamensis; Poaceae) in Taiwan. Molecular Ecology 8: 263-270.
Jung, J. Singh, SK. Pande, HC. Srivastava, GK and Choi, HK. 2014. Genetic diversity and population structure of Indian Isoëtes dixitei Shende based on amplified fragment length polymorphisms and intron sequences of LEAFY. Aquatic Botany 113: 1-7.
Keiper, FJ and McConchie, R. 2000. An analysis of genetic variation in natural populations of Sticherus flabellatus [R. Br. (St John)] using amplified fragment length polymorphism (AFLP) markers. Molecular Ecology 9: 571-581.
Kim, C. Na, HR and Choi, HK. 2008. Conservation genetics of endangered Brasenia schreberi based on RAPD and AFLP markers. Journal of Plant Biology 51: 260-268.
Kim, C. Kim, H and Choi, HK. 2011. Assessment of the minimum population size for ex situ conservation of genetic diversity in Aster altaicus var. uchiyamae populations inferred from AFLP markers. Korean Journal of Environment and Ecology 25: 470-478 (In Korean).
Kim, C. Na, HR. Jung, J. Kim, H. Hyun, Jo. Shin, H and Choi, HK. 2012. Determination of the minimum population size for ex situ conservation of water-shield (Brasenia schreberi J.F. Gmelin) inferred from AFLP analysis. Journal of Ecology and Environment 35: 1-6.
Kong, WS. 1985. A Phytogeographical Study on the Distribution of Bamboos in the Korean Peninsula. Journal of Ecology and Environment 8: 89-98 (In Korean).
Kong, WS. 2001. Spatio-Temporal Distributional Changes of Bamboo. Journal of Korean Geographical Society 36: 444-457 (In Korean).
Lee, TB. 2003. Colored Flora of Korea. Vol. III. Hyangmunsa, Seoul. (In Korean).
Lee, WT and Yim, YJ. 1978. A study on Distribution of Vascular Plant in Korea. Journal of Plant Biology 8: 1-33.
Lee, YN. 2006. New Flora of Korea. Kyohaksa, Seoul. (In Korean).
Loveless, MD and Hamrick, JL. 1984. Ecological determinants of genetic structure in plant populations. Annual Review of Ecology and Systematics 15: 65-95.
Mantel, N. 1967. The detection of disease clustering and a generalized regression approach. Cancer Research 27: 209-220.
Martin, PR and McKay, JK. 2004. Latitudinal variation in genetic divergence of populations and the potential for future speciation. Evolution 58: 938-945.
Miller, MP. 1997. Tools for Population Genetics Analysis (TFPGA). A Windows program for the analysis of allozyme and molecular population genetic data, ver. 1.3. Department of Biological Sciences. Northern Arizona University, Flagstaff, AZ.
Moran, GF. Bell, JC and Turnbull, JW. 1989. A Cline in Genetic Diversity in River She-Oak Casuarina cunninghamiana. Australian Journal of Botany 37: 169-180.
Nakai, T. 1952. A Synoptical Sketch of Korean Flora. Bulletin of the National Science Museum, Tokyo. 143 pp.
Nakajima, M. K, N. a, and Fujio, Y. 1991. Fluctuation of gene frequency in sub-populations originated from one guppy population. Bulletin on the Japanese Society for the Science of Fish 57: 2223-2227.
Nei, M. 1973. Analysis of gene diversity in subdivided populations. Proceedings of the National Academy of Sciences of the United States of America 70: 3321-3323.
Nei, M. 1978. Estimation of average heterozygosity and genetic distance from a small number of individuals. Genetics 89: 583-590.
Schrey, AW. Grispo, M. Awad, M. Cook, MB. Mccoy, ED. Mushinsky, HR. Albayrak, T. Bensch, S. Burke, T. Butler, LK. Dor, R. Fokidis, HB. Jensen, H. Imboma, T. Kessler-Rois, MM. Marzal, A. Stewart, IRK. Westerdahl, H. Westneat, DF. Zehtindjiev, P and Martin, LB. 2011. Broad-scale latitudinal patterns of genetic diversity among native European and introduced house sparrow (Passer domesticus) populations. Molecular Ecology 20: 1133-1143.
Suyama, Y. Obayashi, K and Hayashi, I. 2000. Clonal structure in a dwarf bamboo (Sasa senanensis) population inferred from amplified fragment length polymorphism (AFLP) fingerprints. Molecular Ecology 9: 901-906.
Tamura, K. Peterson, D. Peterson, N. Stecher, G. Nei, M and Kumar, S. 2011. MEGA5: Molecular Evolutionary Genetics Analysis using Maximum Likelihood, Evolutionary Distance, and Maximum Parsimony Methods. Molecular Biology and Evolution 28: 2731-2739.
Tian, B. Yang, HQ. Wong, KM. Liu, AZ and Ruan, ZY. 2012. ISSR analysis shows low genetic diversity versus high genetic differentiation for giant bamboo, Dendrocalamus giganteus (Poaceae: Bambusoideae), in China populations. Genetic Resources and Crop Evolution 59: 901-908.
Triplett, JK. Oltrogge, KA and Clark, LG. 2010. Phylogenetic relationships and natural hybridization among the North American woody bamboos (Poaceae: Bambusoideae: Arundinaria). American Journal of Botany 97: 471-492.
Tsuyama, I. Nakao, K. Matsui, T. Higa, M. Horikawa, M. Kominami, Y and Tanaka, N. 2011. Climatic ontrols of a keystone understory species, Sasamorpha borealis, and an impact assessment of climate change in Japan. Annals of Forest Science 68: 689-699.
Vos, P. Hogers, R. Bleeker, M. Reijans, M. Lee, T. Hornes, M. Friters, A. Pot, J. Paleman, J and Kuiper, M. 1995. AFLP: a new technique for DNA fingerprinting. Nucleic Acids Research 23: 4407-4414.
Yeh, FC. Yang, RC. Boyle, TB. Ye, ZH and Mao, JX. 1997. POPGENE, the user-friendly shareware for population genetic analysis. Molecular Biology and Biotechnology Centre University of Alberta; Edmonton, Alberta.
Yim, YJ and Kira, T. 1977. Distribution of forest vegetation and climate in the Korean peninsula III. Distribution of tree species along the thermal gradient. Japanese Journal of Ecology 27: 177-189.
Zhang, W and Clark, LG. 2000. Phylogeny and classification of the Bambusoideae (Poaceae). In Grasses: Systematics and Evolution. Jacobs, S. W. L., J. Everett (eds.). Csiro Publishing, Australia. 35-42.
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||