지구상의 약 30만 종의 식물 종 중 많은 종들이 인간 활동의 확대로 인한 서식지의 분절화 및 파괴, 외래종 도입에 따른 경쟁, 그리고 남획 등으로 인하여 생존을 위협받고 있다. 국제자연보전연맹(International Union for Conservation of Nature and Natural Resources; IUCN)은 1966년부터 절멸 가능성이 있는 야생생물의 적색목록(Red List)을 만들어 공표하고 있으며, 2015년의 통계에 의하면 20,755종의 식물이 적색목록에 등재되었다(IUCN, 2015). 우리나라에서도 1991년에 제정한 자연환경보전법에 처음 관련 내용을 포함하였고, 이후 2004년에 제정한 야생동식물보호법 및 2014년 개정된 생물다양성이용 및 보전에 관한 법률에 따라 멸종위기야생동식물을 관리하고 있다.
난초과(Orchidaceae)는 식물계의 종 수가 많은 과 중 하나로, 약 19,500−25,000종이 세계적으로 분포한다(Dressler, 1993). 난과 식물들은 꽃의 아름다움과 그 향으로 인해 남획의 대상이 되어왔으며, 그 결과 많은 종들이 멸종위기에 처했다. 따라서 무분별한 남획을 방지하기 위하여 난과 식물의 모든 종들은 국제적으로 상업적 거래가 금지되어있다(CITES, 2013). 단 인공 증식한 개체들만 관리기관의 허가 아래 국제적 거래가 허용되고 있을 뿐이다. 또한 IUCN의 적색목록에 등재된 식물 가운데 837종이 난과 식물로, 전체 등재된 식물의 약 4%를 차지하고 있다. 적색목록에 등재된 식물들 중 절멸되었거나 절멸되었을 것으로 추정되는 식물은 818종이며, 그 중 난과 식물이 380종으로 약 46%를 차지하고 있다. 식물의 과가 400여개 이상인 점을 고려하여 볼 때 이는 단일 과로써는 압도적인 비중이다.
우리나라의 경우, 환경부가 법적 보호종으로 지정한 식물 종은 1급 9종과 2급 68종으로 총 77종이다. 그 중에서 난초과 식물은 1급 6종, 2급 13종으로 총 19종이다(Ministry of Environment, 2012). 이는 우리나라 멸종위기식물의 24%를 차지한다. 자생종 88종(Lee et al., 2007) 중, 19종이 멸종위기종으로 멸종위기종의 비율은 22%로 다른 식물의 과에 비하여 압도적으로 높다. 이는 우리나라 난과 식물의 약 20%가 멸종위기종으로 지정되어 있고, 우리나라 멸종위기종 전체의 25%가 난과 식물이라는 이야기이다. 따라서 멸종위기 식물종의 보존과 관리에서 난과 식물이 그 핵심에 있다고 강조하여도 과하지 않다.
우리나라에서 난과 식물은 다른 과 식물들에 비하여 주요 멸종원인도 다르다. 다른 식물들은 서식지 분절화 및 파괴, 외래종과의 경쟁에 따른 서식지 감소가 주요 멸종 원인인 경우가 많으나, 난과 식물은 관상 가치로 인한 남획이 주요 멸종원인인 경우가 대부분이다. 또한 난과 식물은 서식지가 좁은 지역으로 제한된 종들이 많고, 서식지 변화에 민감하게 반응한다. 따라서 난과 식물을 보존 하고 복원하는 일은 우리나라 멸종위기 식물종의 복원에서 가장 중요한 비중을 차지한다. 난과 식물은 서식환경에 따라 다른 식물이나 암석 등에 부착하여 살아가는 착생란과 토양에 뿌리를 박고 살아가는 지중성난으로 대별할 수 있다. 우리나라 멸종위기종 난 중 풍란, 석곡, 나도풍란, 금자란, 지네발란, 비자란, 차걸이란, 탐라란, 콩짜개란 등 9종은 착생란이다. 반면 한란, 백운란, 죽백란, 대흥란, 복주머니란, 털복주머니란, 광릉복주머니란, 으름난초, 구름병아리란, 해오라비난 등 10종은 지중성난이다. 대부분의 난과 식물은 종자에 배유가 없어서 종자발아를 위하여 서식지의 공생근균의 도움을 받아야 한다(Rasmussen, 1995). 그러므로 난과 식물의 종과 공생근균의 관계를 정확하게 이해하기 전에는 자연 상태에서 종자증식이 어렵다. 또한 종자증식이 가능하다고 하여도 종자가 발아하여 자라는 확률은 매우 낮다. 따라서 난과 식물의 대량증식을 위해서는 인공배지에서 배양하는 기술이 확보되어야한다. 난과 식물을 증식하는 방법에는 조직배양과 종자를 이용한 배아배양 방법이 있다. 그러나 복원을 위한 증식에는 유전적 다양성이 확보될 수 있는, 종자를 이용한 배아배양방법이 주로 이용된다.
국내외적으로 멸종위기 난과 식물 종을 복원하는 것은 멸종위기 식물종 복원의 주요 의제이다. 그러나 성공적인 복원사례는 그리 많지 않다. 제한적이지만 복원사례를 보면, 인도에서 Ipsea malabarica Hook. f. 및 Vanda coerulea Griff. ex Lindl. (Seeni and Latha, 2000; Martin, 2003)을, 싱가포르에서 Grammatophyllum speciosum Blume (Yam et al., 2010)을, 호주에서 Caladenia huegelii Rchb. f., Diuris fragrantissima D.L. Jones & M.A. Clem. (Smith et al., 2007, Swarts et al., 2007)을 복원한 예가 있다. 우리나라에서는 2006년 풍란 15,000여 촉이 관매도에 복원된 바 있고(Shin et al., 2009), 2011년에 국립수목원에서 제주도에 탐라란 300개체를, 2011년에 완도수목원 내에 석곡 300개체를, 2013년에 국립수목원에서 한라산국립공원에 금자란 250주를, 그리고 2015년에 국립공원관리공단에서 한려해상 국립공원에 풍란 500개체를 복원한 바 있다. 그러나 풍란 복원 사례를 제외하고 우리나라의 복원사례는 대부분 단편적인 뉴스로만 보도되었고, 증식, 복원, 복원 후 모니터링 전 과정을 정리한 논문은 발견하기 어려운 상태이다. 따라서 본 연구에서 수행한 석곡의 복원 사례를 논문으로 정리하는 것은 의미가 크다.
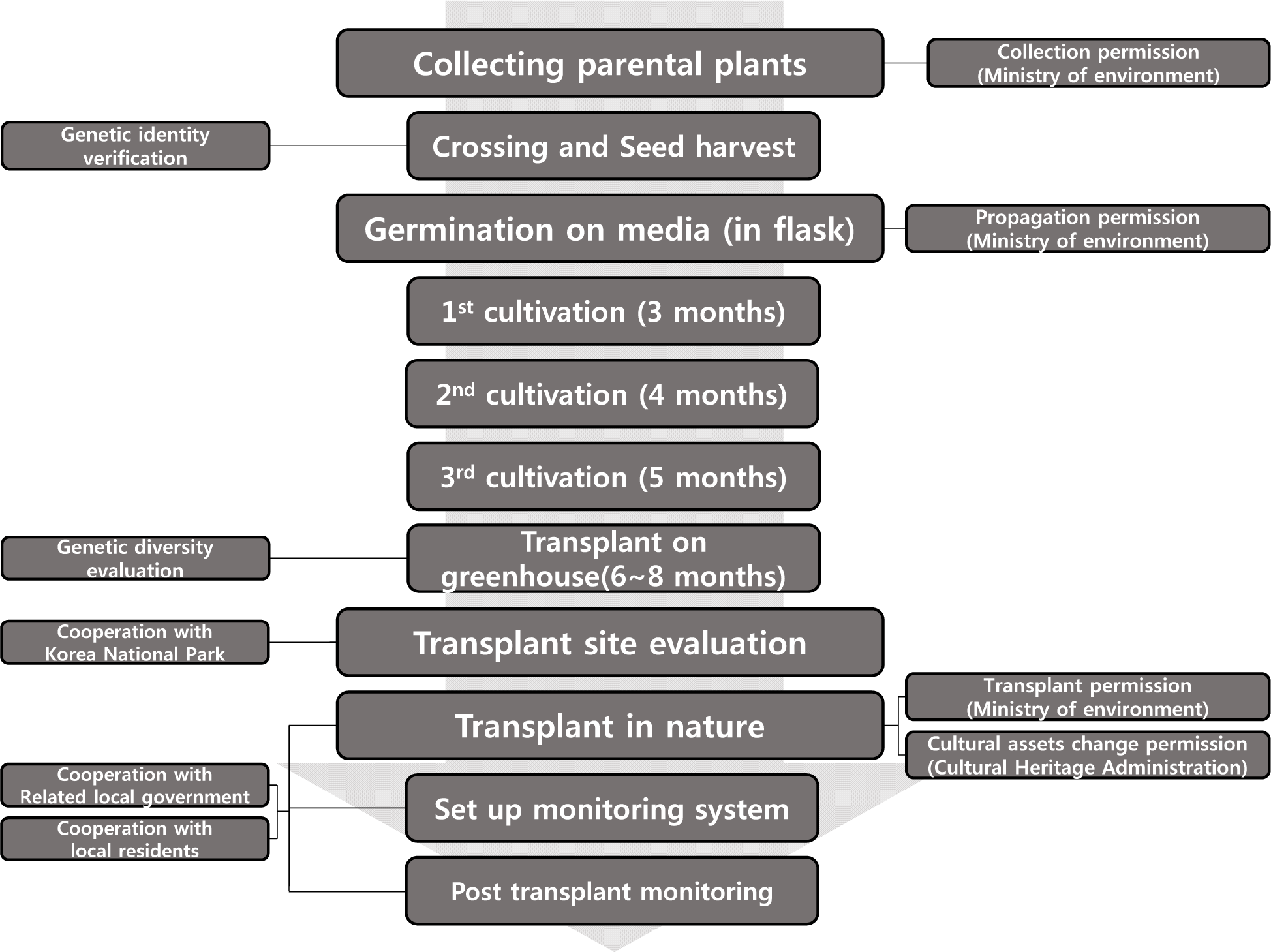
본 연구는 복원 대상종으로 선정한 석곡(Dendrobium moniliforme (L.) Sw.)의 대량증식과정과 생태계 복원과정, 복원 후 2년간의 모니터링 결과를 정리하였다. 전체 소요된 연구 기간은 7년이다. 모본수집에서 종자형성, 플라스크에서 3단계의 기내배양, 온실에서의 순화배양, 배양된 개채들의 유전적 다양성 검증, 복원지의 선정, 야생으로의 복원, 복원 이후 2년 간의 성장률, 번식률, 개화 및 결실의 과정을 추적하여 자료화 하였다. 단계마다 수반되는 관리기관의 허가, 지역주민들이 참여하는 복원 및 모니터링과정을 하나의 논문으로 보고한다. 이 논문은 앞으로 우리나라 멸종위기 식물종의 복원에 대한 기획 및 실행과정에 참고자료가 될 것이다.
재료 및 방법
모본의 확보 및 유전자검증
모본의 확보: 복원에 사용된 석곡(D. moniliforme)의 모본은 석곡이 멸종위기종으로 지정되기 전인 2008년 7월 전라남도 진도에서 채집된 것이다. 한 농부가 전라남도 진도 관매도에서 자연 채취하여 매매하려고 한 2개의 개체를 지역 환경단체 회원들이 회수하여 연구진에게 연구 목적으로 기증하였다. 이 개체는 DNA 검증을 통하여 우리나라 개체임을 확인하였다(Kim et al., 2015). 석곡이 2012년 멸종위기종으로 고시됨에 따라, 실험이 진행되는 과정에서 2012년 한강유역환경청에 기존 획득 신고와 인공증식 허가를 받았다.
유전자검증: 모본의 유전적 평가 및 증식한 개체들의 유전적 다양성 분석을 위하여 핵 유전체와 엽록체 유전체의 일부구간 등 5개 지역을 분석하였다. 검증마커로 이용된 지역은 nrITS, matK, rbcL, psbA-trnH, atpF-atpH, psbK-psbI 지역이다 (White et al., 1990; CBOL Plant Working Group, 2009). 개체들에서 잎을 채취하여 DNeasy plant mini kit (Qiagen, Germany)를 이용하여 DNA를 추출하여 한국의식물 DNA은행(Plant DNA Bank in Korea)에 보관 중인 DNA 시료 (PDBK-2013-1829, 2013-1830, 2013-1831, 2013-1837) 로부터 PCR을 수행하였다. PCR 산물은 PCR 정제 키트 (iNtRON Biotechnology)를 이용하여 정제하였다. 정제된 PCR 산물은 ABI3730xl DNA sequencer로 염기서열을 결정하여(Applied Biosystems) Geneious Pro 6.1.8 (Biomatters Ltd.)를 이용해 정렬하였다. 정렬된 염기서열은 MEGA6 (Tamura, 2013)을 이용해, Kimura’s two-parameter method (Kimura, 1980)로 유전적 거리 값을 얻어 비교 분석하였다.
대량증식
자생지에서 취득한 석곡모본들을 온실에서 육성한 결과 2009년 3월에 개화하였다. 두 개체에서 각각 꽃 30개씩을 선정하여 화분채취를 위해 수그루 15개, 암그루 15개를 수분시켰다. 인공수분 후 4개월 후에 10개의 꼬투리가 성공적으로 성숙하였다. 이중 가장 건실한 4개의 꼬투리를 2009년 8월 삭과가 벌어지기 전에 수확하여 겉을 90% 에탄올로 소독 후 멸균후드에서 열어서 Kano배지에 파종하였다. 3개월간 발아배지에서 발아시킨 어린 배아를 2009년 12월 생육배지가 든 삼각플라스크에 접아하고, 23˚C, 2,000 Lux, 광주기 16/8시간의 상태에서 6개월간 1차 무균배양하였다. 2010년 6월 생육배지로 이식하였다. 생육배지로는 1 리터 당 Hyponex, Peptone, Sucrose, Charcoal 을 각각 3 g, 2 g, 30 g, 0.5 g 혼합한 배지를 pH 범위 5.6−5.8 로 조정하여 사용하였다. 무균배양한 개체는 1 L 당 바나나, 감자, 사과가 각각 30 g, 30 g, 20 g 들어간 배지에 이식하여 3개월, 4개월, 5개월 간 각각 배양하였다.
총 12개월간 배양을 거친 개체는 2011년 6월 105공 플러그판에 물이끼 수태를 이용하여 이식하였다. 플러그판에 이식된 개체는 습도 80−90%, 온도 22±2˚C, 3,000−4,000 Lux 의 광선이 이중차광된 조건의 온실에서 순화과정을 거쳤다. 수태식재 후에는 살균제(베노밀)를 이용하여 살균하였으며, 순화배양 2주 후부터는 Hyponex (N:P:K=6:7:19)를 2,000배 희석하여 엽면에 시비하였다. 12개월간 온실에서 순화과정을 거친 개체는 2형포트에 옮겨 1년을 더 키운 후 2013년 6월 자연복원에 이용하였다.
복원지 선정 및 사전준비
우리나라 남해안 일대의 식생이 우수한 상록수림 지역 중 석곡이 생육 가능한 자연환경조건(식생, 온도, 습도)을 기준으로 경상남도 거제도 북병산 일대, 경상남도 남해도 금산 일대, 전라남도 완도군 구계등 일대, 전라남도 외나로도 봉래 상록수림 일대, 전라남도 목포시 유달산 일대, 전라남도 완도군 보길도 일대 등 총 6개 지역을 조사지역으로 선정하여 2012년 6−10월에 걸쳐 방문하여 입지를 평가하였다. 6개 대상지역 중에서 주위 식생과 기온 및 습도를 고려하여, 복원대상 난들의 생존 가능성이 높은 경상남도 남해도 금산 일대, 전라남도 외나로도 봉래 상록수림 일대, 그리고 전라남도 완도군 보길도 일대의 총 3개 지역이 1차 복원 후보지로 선정되었다. 2013년 4월 중 1차 선정지 세 곳을 2차 방문하여 착생 난을 부착시킬 기주식물을 포함한 식생분석, 자연환경 요인분석, 복원 이후 관리의 수월성, 복원의 대국민 교육효과, 지역주민들의 참여의지 등을 고려하여 국립공원지역이고 상시 관리가 가능한 완도군 보길도 부용동 일대를 최종 선정하였다.
최종 선정된 보길도 부용동 세연정 및 보길저수지 일대를 2013년 4월 16일 연구진들과 국립공원관리공단 직원들이 방문하여 정확한 복원지와 착생 기주식물들의 종류 및 수, 각 식물 당 부착할 난의 수를 결정하였다. 복원 이후 채취를 가장 효과적으로 차단할 수 있고 난 생육에 필수 적인 습도가 높은 수자원보호지역인 보길저수지 일대의 가상 복원지도를 작성하였고, 문화재보호지역인 세연정 일대는 문화재청에 멸종위기종 복원을 위한 현상변경신청을 완료하였으며, 국립공원관리공단과는 멸종위기종 복원을 위한 업무협약을 체결하여 복원 이후 사후 관리를 국립공원이 주관하도록 하였다. 또한 복원을 위하여 영산강유역환경청에 멸종위기종 복원허가, 완도군청에 행정 협의 및 보길면에서 지역 주민들의 참여를 위한 설명회를 개최하였다.
복원, 관리 및 모니터링
복원할 개체들은 약 10여 촉을 한 묶음으로 수태로 뿌리를 쌓아 묶은 후 현장으로 이송하였다. 이송된 개체들은 2013년 6월 21일에 지역주민들과 함께 보길면 세연정 일대에 복원하였다. 주로 나뭇가지에 부착시킨 후 수분 보존을 위하여 마대포대로 감싸고 묶어 주는 방법으로 이식하였다. 세연정 일대에는 기주식물을 다르도록 하여 약 4,000 촉을 이식하였다. 2013년 6월 22일에는 연구진과 구립공원 직원들이 참여하여 민간인 출입이 통제되는 보길저수지 일대의 상수도 보호지구에 9,000 촉을 이식하였다. 보길저수지 지역에는 식물에 부착하는 방법과 바위틈에 이식하는 방법을 동시에 수행하였다. 나무에 부착은 7 m 사다리를 이용하여 3인이 1조가 되어 복원하였으며, 복원하는 개체들은 약 10여촉을 한 묶음으로 하여 복원되었다. 복원 이후 사후관리를 위하여 복원지역에 표지판과 cctv를 설치하여 출입을 관리하였다. 복원 후 1년, 2년 뒤인 2014년 6월 25일, 26일과 2015년 6월 9일, 10일 양일간 복원지를 방문하여 복원한 석곡의 1년간의 생육상태를 모니터링하였다. 모니터링을 위하여 석곡 개체의 구 촉수, 신 촉수, 촉 길이의 최소값, 중간값, 최대값을 조사하였다. 복원한 석곡의 개화, 결실, 고사율과 기주식물명, 기주식물의 수고 및 직경을 함께 기록하였다.
결 과
모본의 확보에서 복원 이후 2년간 모니터링에 이르는 7년간의 연구 과정은 Fig. 1에 요약하였다.
먼저 획득한 모본간에 인공 수정시켜 육성한 종자를 채취하여 조직배양실에서 기내파종하였다(Fig. 2A, B). 파종 후 발아한 유모를 6개월간 배양한 뒤, 12 개월 간 3단계로 다른 플라스크에 이식하여 계대배양하였다(Fig. 2C, D). 12개월간 배양한 개체가 3−4 cm 크기로 자라나면 플러그 판에 물이끼 수태를 이용해 이식하여 온실에서 순화, 육묘하였다. 총 13,000 촉의 석곡이 증식되었으며, 2형포트에 다시 이식하여 자연복원에 이용할 수 있도록 준비하였다(Fig. 2E, F). 원래는 2012년 10월에 복원하려 하였으나 10월 복원 이후 활착이 덜 된 상태에서 추운 겨울을 맞을 경우 고사율이 높을 것으로 예견하여, 복원시기를 2013년 봄철 건기를 넘긴 후 6월로 재조정함에 따라 8개월을 온실에서 더 생육하였다. 따라서 복원에 이용된 개체들은 모두 완전한 성체로 성장하여 일부개체들은 온실에서 꽃을 피운 상태로 복원에 이용하였다.
석곡의 자연복원은 2013년 6월 21일, 22일 양일에 걸쳐 이루어졌다. 연구진을 비롯하여 국립공원관리공단 직원, 생물자원이용기술연구단 일원, 그리고 지역 주민 등 총 150여명이 참여하여(Fig. 2G, H, I), 13,000 촉을 전남 보길도 세연정 주변 및 보길저수지 인근에 복원하였다. 자연 복원지의 기주식물은 흉고직경 30 cm 이상의 소나무(Pinus densiflora Siebold & Zuccarini), 동백나무(Camellia japonica L.), 붉가시나무(Quercus acuta Thunb.), 후박나무(Machilus thunbergii Sieb. et Zucc.), 모밀잣밤나무(Castanopsis cuspidata var. thunbergii Nakai), 예덕나무(Mallotus japonicus (Thunb.) Muller-Arg.), 등이다. 기주식물에 10여 촉씩 한 묶음으로 목공 본드로 부착하여 녹화마대로 뿌리부위를 감싸고 끈으로 묶는 방법이다. 일부 개체는 돌틈에 호미로 심고, 뿌리가 활착하기 용이하도록 물이끼류로 덮어 이식하였다(Fig. 2J). 보길저수지 인근의 식생과 미세기후에 따라, 복원장소를 세 군데로 세분할 수 있다. 물가와 가깝고 햇빛이 비교적 강하게 들어오는 저수지 가장자리부분, 물가와 멀고 해가 잘 들어오지 않 는 상록수림 안쪽, 그리고 저수지를 둘러 난 임도 가까이로 나누어 복원되었다.
복원 전에 증식된 석곡 개체들의 유전적 다양성을 검증하기 위하여 복원할 개체 3개를 임의로 선정하여 모체와 함께 개체들의 유전적 다양성을 평가하였다. rbcL지역의 genetic distance 값은 0.0902%, psbK-psbI 지역의 genetic distance 값은 0.8008%이었으며 matK 지역과 psbA-trnH 지역, atpF-atpH 지역, nrITS 지역은 변이가 없었다. psbK-psbI 지역, rbcL지역, atpF-atpH 지역에서 각각 9개, 1개, 1개의 염기치환 및 indel을 발견하였다. 특히 psbK-psbI 지역의 경우 6개 염기치환과 3개의 indel을 발견하였으며, 앞으로 석곡의 유전적 다양성을 평가하는데 최적의 마커로 평가 된다(Fig. 3).
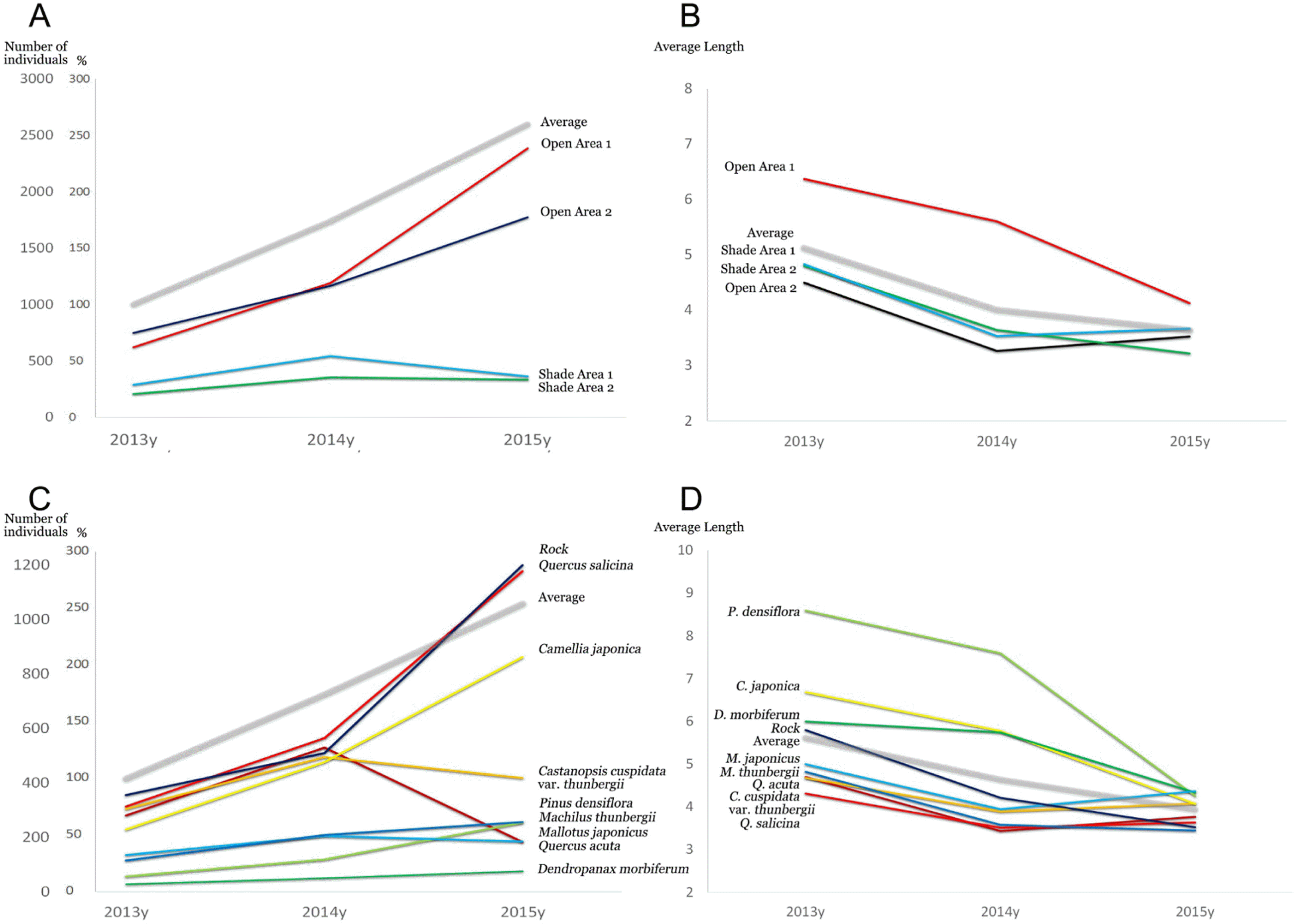
2013년 6월 복원 1년 후(2014년 6월), 복원 2년 후(2015년 6월)등, 두 차례에 걸친 모니터링조사의 결과로 복원한 석곡 개체들이 잘 생장하고 있음을 확인할 수 있다(Fig. 4A, B, C, D, E, F, G, H, I, J). 2013년에 대비하여 2014년에는 176.5%의 영양번식률을, 2015년에는 226.9%의 영양번식률을 보였다(Fig. 5A, C). 구 촉의 길이, 신 촉의 길이를 조사한 결과는 다음과 같다. 2014년에 조사한 구 촉의 중간값 길이의 평균은 5.13 cm로, 같은 해 조사한 신 촉의 중간값 길이 평균은 2.9 cm로 나타났다. 2015년에 조사한 구 촉의 중간값 길이의 평균은 5.29 cm로 전년보다 약간 증가하였으며, 신 촉의 중간값 길이 평균은 1.99 cm로 나타났다(Fig. 5). 전체 길이의 평균을 장소별로 조사한 결과에 따르면 복원 당시는 5.13 cm, 2014년에 4.01 cm, 2015년에 3.64 cm로 나타났다(Fig. 5B, D). 기주식물별로 조사한 결과에 따르면 복원 당시는 5.62 cm, 2014 년에 4.64 cm, 2015년에 3.95 cm를 기록하여 전체적인 길이가 감소하는 경향을 보였다.
장소별로 나누어 확인하였을 때 번식률이 가장 높은 곳은 384.4%를 기록한 세연정 인근이었고, 가장 낮은 곳은 125.4%를 기록한 저수지 임도였다(Fig. 5A). 기주식물별 로는 붉가시나무(Q. acuta)가 65.4%로 가장 낮은 번식률을 보였고, 참가시나무(Quercus salicina Blume)가 375.5%로 가장 높은 번식률을 보였다(Fig. 5C).
2014년에 저수지 가장자리에서 조사한 석곡 개체들이 구 촉 4.5 cm, 신 촉 2.04 cm로 가장 짧은 길이생장을 보였으며, 2015년에는 저수지 숲 속에서 확인한 개체들이 구 촉 4.84 cm, 신 촉 1.6 cm로 가장 짧은 길이를 기록하였다(Fig. 5B). 기주식물별로는 2014년에는 참가시나무(Q. salicina)와 붉가시나무(Q. acuta)가 각각 구 촉 4.32 cm, 신 촉 2.18 cm로 가장 짧았다. 2015년에는 후박나무(M. thunbergii)에 복원된 개체들이 구 촉 5.07 cm, 신 촉 1.84 cm로 가장 짧았다(Fig. 5D).
2014년도 조사에서 세연정 동백나무(C. japonica)에 복원한 석곡 개체에서 개화와 종자 결실을, 세연정 소나무(P. densiflora)에서 종자 결실을, 저수지 임도의 붉가시나무(Q. acuta)에서 개화를 확인하였다. 2015년 조사에서는 종자 결실은 확인할 수 없었으나 세연정의 예덕나무(M. japonicus)에 복원한 개체로부터 개화를 확인하였다. 2014년 조사에서 81 촉, 2015년 조사에서 102 촉의 고사한 석곡 개체를 확인하였다. 두 조사에서 공통적으로 바위에 복원한 개체들이 많이 고사하였다. 2014년의 조사에서 죽은 개체들이 모두 바위 표면에 복원된 개체들이었던 것에 비해, 2015년의 조사에서 죽은 개체들은 동백나무(C. japonica), 때죽나무(Styrax japonicus Siebold & Zucc.), 소나무(P. densiflora), 모밀잣밤나무(C. cuspidata var. thunbergii)에 복원된 것들로 확인되었다.
복원지 보존을 위하여 복원지에 안내판을 설치하였고, 태양광에 의하여 자동 작동되는 감시카메라 시스템을 설치하였으며, 국립공원 사무실에서 상시 모니터링이 가능하다. 또한, 사람이 접근할 경우 경고 방송이 나가는 감시 시스템을 운영중이다. 또한 동네 주민들과 국립공원관리 사무소 보길분소의 직원들이 협동으로 복원지 부근의 외부인의 출입을 감시하는 체계를 구축하여 운영 중이다.
고 찰
본 복원 연구에서 증식된 석곡 개체는 총 13,000 촉이다. 단일 종의 복원사업으로는 관매도에 풍란 15,000 촉을 이식한 이후로(Shin et al., 2009) 국내 최대 규모의 멸종위기종 복원사업이다. 국외의 난과 식물 복원 사례를 살펴보아도 1만 촉 이상의 대규모 복원사업은 찾아보기 힘들다. 국내 난과 식물 복원 사업이 모두 착생란을 대상으로 한 것에 비교하면, 해외 난과 식물 복원의 대부분은 지중성난을 대상으로 하고 있다(Stewart, 2008).
복원을 위하여 13,000 촉의 석곡은 종자번식으로 증식한 개체들이어서 유전적으로도 다양한 개체들이다. 4개의 개체를 임의로 선정하여 국내 다른 지역의 석곡 15개체와 유전적 다양성을 비교하였을 때, rbcL 지역은 국내 평균 유전적 거리보다 높게 나타났고, psbK-psbI지역은 비슷한 값을, 나머지 지역은 낮은 값을 보였다. 다만 복원 개체의 atpF-atpH, matK, rbcL, trnH-psbA 지역으로부터 얻어진 유전적 거리 값은 전체 국내 유전적 거리 값의 표준편차 범위 내에 포함되며, 그렇지 않은 nrITS 지역의 유전적 거리 값도 2σ범위 내에 포함된다. 이는 더 많은 복원 개체를 검증하였을 경우, 복원 개체들의 유전적 다양성이 국내 개체들의 유전적 다양성과 비슷한 값을 나타낼 것임을 의미한다. 따라서 복원한 개체들의 유전적 다양성은 보장되었다는 결론이다.
2014년, 2015년 두 차례에 걸친 모니터링 결과에 따르면, 조사된 고사한 석곡 개체의 촉수는 각각 81, 102 촉이다. 따라서 복원 당시에 비하여 각각 97.5%, 97.9%의 높은 생존율을 기록하고 있다. 고사한 개체의 대부분은 저수지 가장자리의 돌 틈에 복원한 것이다. 해당 지역이 저수지와 인접하여 직사광선을 막아줄 수 있는 식생이 부족한 것과 직사광선에 돌들이 달구어져 온도가 올라간 것이 석곡의 고사를 유발한 것으로 추측된다. 반대로, 그늘이 지는 바위틈에 복원한 석곡 개체들은 높은 번식률을 기록하였다(Fig. 5C). 다른 지역에서 고사한 복원 개체들의 경우, 부착한 가지가 썩거나 태풍에 따른 바람의 영향을 받아 제대로 착생하지 못하고 떨어져 죽은 것들이 대부분이었다.
Yam et al. (2010)은 착생란인 Grammatophyllum speciosum을 싱가포르의 다양한 지점에 복원하고 그 생존률을 보고 하였는데, 기주식물과 지역에 따라 낮게는 25%에서 높게는 95%를 기록하였다. Seeni and Latha (2000)는 인도에서 착생란인 Vanda coerulea를 복원하고 그 생존률을 보고하였다. 기주식물, 장소, 복원방법에 따라 75%에서 100%의 생존율을 기록하였다. 두 사례에서 복원에 사용한 유묘의 수가 40개 이하로 작은 것을 고려하더라도, 이번에 복원된 석곡의 생존율은 비교적 높은 것으로 평가된다.
장소별, 기주식물별로 기록한 촉 수, 길이 변화를 그래프로 나타낸 것은 Fig. 5와 같다. 장소별 촉 수 변화 그래프를 살펴보면 전체적으로 촉수가 증가하는 것을 확인할 수 있다. 특히 개활지인 세연정과 저수지 가장자리에서의 번식률이 음지인 저수지 임도와 숲 속보다 월등하게 높았다. 비록 직사광선이 직접적으로 들어오는 저수지 가장자리의 바위 근처에 복원된 일부 개체들은 고사하였지만, 저수지 인근의 빛이 어느 정도 들어오는 나무에 부착한 개체들이 성공적으로 번식하여 전체적으로 높은 번식률을 보였다.
저수지 숲 속에서는 예년과 비슷한 개수의 복원 개체가 확인되었지만, 저수지 임도에서는 예년보다 적은 수의 석곡 촉수를 기록하였다. 2015년 조사에서 저수지 임도와 저수지 숲 속에 복원한 석곡 개체 일부가 땅에 떨어진 것을 발견하였는데, 아마도 태풍 피해의 영향으로 추측된다. 가장 낮은 번식률을 보인 기주식물은 황칠나무(Dendropanax morbidera Lev.)이고, 다음이 붉가시나무(Q. acuta), 센달나무(Machilus japonicus Sieb. et Zucc.) 순이었다. 이들 3개 종을 제외한 나머지 8개 기주식물에서는 모두 137%가 넘는 번식률을 기록하였다. 반대로 가장 높은 번식률은 저수지 부근의 그늘진 바위틈과 참가시나무(Q. salicina) 수피에 복원한 개체들에서 관찰되었는데, 300% 이상의 영양번식률을 보여주었다. 다음으로 성공적인 기주식물은 동백나무(C. japonica)의 순이었다. 붉가시나무와 참가시나무 기주식물의 경우 같은 속임에도 큰 차이를 보이는 것은 붉가시나무의 잎이 넓고 수관이 빽빽하여 줄기에 빛이 거의 도달하지 않은 반면, 참가시나무의 경우는 잎이 작고 수관이 덜 밀집되어 있어서 어느 정도의 광량이 줄기에 도달하는 차이 때문인 것으로 생각된다. 석곡은 너무 빛이 강해도 생존이 어렵지만 빛이 너무 약해도 번식이 어려우며, 그늘이 지지만 어느정도 광이 투시되는 반음지 지역이 생존 적지로 판단된다. 양지의 바위틈에 복원한 개체는 대부분 고사하였으나, 그늘진 바위틈에 복원한 개체들이 참가시나무에 복원한 개체들과 비슷한 수준으로 왕성하게 영양번식한 것도 이를 뒷받침한다(Fig. 5A, C). 또한 줄기에 빛이 많이 투시되는 세연정의 소나무(P. densiflora)에 복원한 개체들에서도 비교적 잘 증식하고 있는 것도 이를 뒷받침한다. 따라서 기주식물에 관계없이 석곡의 반음지습성에 비슷한 환경 조성이 중요한 것으로 판단된다.
전반적인 촉 수 증가에 따른 증식률의 증가와는 반대로 복원 후 시간이 갈수록 각 촉의 평균 길이는 짧아지는 것을 확인할 수 있었다(Fig. 5B, D). 새로운 촉이 적게 번식하였거나, 기존에 있던 촉이 길게 생장한 몇 가지 경우에는 길이가 약간 증가하는 경향을 보였다. 그러나 대부분의 경우 평균 길이가 짧아졌으며, 이는 복원 원년에는 온실에서 잘 성장한 개체를 이용하였으나, 복원 1년, 2년 후의 6월은 아직 새 촉의 생장 초기 단계이기 때문으로 생각된다. 즉, 복원된 개체로부터 새로운 촉이 왕성하게 번식함에 따라 복원 원년의 긴 길이에 비해 촉 길이의 중간 값이 줄어들었기 때문이다. 그러나 앞으로 모니터링을 계속하고 복원 원년의 촉들이 고사하면 촉의 평균 길이 값은 안정될 것으로 예측된다.
난 종류는 다른 식물에 비하여 서식지가 제한적이며 서식환경에 보다 더 민감하게 작용한다. Swarts and Dixon (2009)은 복원 대상지가 복원 대상종의 조건과 얼마나 잘 부합하는지, 토양 조건이 잘 맞는지, 지형은 어떤지, 그리고 수리학적 조건은 어떤지가 복원 대상종의 원활한 정착과 생존에 중요할 것이라고 이야기한다. Yam et al. (2010)은 상대습도와 같은 미소기후, 기주식물의 질감, 다른 착생 종의 유무 그리고 유묘의 크기가 중요한 요인이라고 언급하였다. 본 연구에서는 복원 석곡 개체들의 높은 생존율과 왕성한 영양번식률이 특징이다. 이는 본래 서식지로 알려진 전라남도 도서지역인 보길도를 복원지역으로 선정한 것, 충분한 시간을 들여 생육한 석곡 개체를 복원에 이용한 것, 복원 시기가 5월의 건기가 끝나고 우기가 시작되기 전에 수행되어 겨울이 오기 전에 충분한 활착기간이 제공된 점, 복원지의 습도가 비교적 높은 점, 지역주민들의 적극적인 보존활동 등이 높은 생존율과 번식률에 영향을 끼쳤을 것으로 판단된다.
복원의 성공에 있어 또 다른 중요한 요인 중의 하나는 개화와 종자 결실이다. 모니터링 결과에 의하면 2014년과 2015년 모두 개화를 관찰하였고, 2014년에는 소나무(P. densiflora)와 동백나무(C. japonica)에 복원한 개체로부터 종자 결실을 확인하였다(Fig. 4G, H). 석곡속(Dendrobium)의 수분은 대부분이 벌에 의해서 이루어지며, 다른 수분 매개자로 꽃등에, 나방, 바구미가 언급되고 있다(Dressler, 1993). 본 연구에서 종자 결실이 이루어진 사실은 복원지 자연 상태에서 석곡의 수분 매개자가 존재함을 입증한다. 그러나 아직까지 종자 전파에 의한 새로운 개체는 발견하지 못하였다. 성공적인 복원이란 복원한 개체들이 야생에서 꽃이 피고 열매를 맺고, 싹이 터서 새로운 개체로 자라는 것이다. 본 복원연구에서 복원 후 1−2년에 종자 결실이 확인되었으므로, 앞으로 새로운 개체가 종자번식으로 발생하는 것이 관찰된다면 성공적인 복원이라 말할 수 있을 것이다. 따라서 앞으로 지속적인 모니터링이 요구된다.
세계적으로 난과 식물이 멸종위기를 맞는 이유는 그 경제적, 관상적 가치로 인한 남획이 큰 요인을 차지하고 있다. 복원 대상종인 석곡(D. moniliforme) 역시 전라남도와 경상남도에 흔하게 자생하였으나 무분별한 채취로 멸종위기에 처하였으며, 사람손이 닿기 어려운 높은 바위틈의 7−8개의 자연서식지만 단편적으로 남아 있을 뿐이다. 복원에 가장 중요한 성공요인이 바로 복원지역의 2차 파괴를 최소화하는 길이다. 이는 연구진과 국립공원관리공단 직원들만으로는 충분하지 못하다. 따라서 인근에서 생활하는 지역주민들의 협조가 복원 이후의 성공적인 정착에 가장 중요한 요인이 된다. 연구진은 지역 주민들과의 면담을 통하여 복원에 대한 참여의지를 확인하여 복원 대상지를 결정하였다. 복원식 준비과정, 복원식 등 연구진의 활동 전반에 걸쳐 지역주민들의 능동적인 참여가 있었다. 복원 후 2년간 단 하나의 개체도 인공적인 훼손이 없음이 이를 잘 뒷받침한다. 복원 개체에 대한 지역 주민들의 끊임없는 관심이 대상 복원지의 보호에 도움이 되고 있다. 그러나 외부인들의 무단 접근과 채취를 막기 위하여 복원 지역에 태양광으로 작동되는 CCTV를 설치하여 국립공원 사무소에서 모니터링하는 2중 보호 수단을 강구하였다. 또한 복원지역이 상수도원 보호구역 및 문화재관리지역이어서 일반인들의 출입이 통제되고 있고 감시체계가 작동하는 것도 도움이 되는 것으로 평가된다.
멸종위기종 석곡의 대량 증식, 적절한 복원지 선정, 지역주민의 참여, 복원 후 모니터링 과정을 통하여 복원된 개체들이 성공적으로 복원지에 정착하는 것을 확인하였다. 앞으로도 중장기적으로 지속적인 조사와 관찰을 통해 복원 이후 종자에 의한 새로운 개체의 증식과정을 관찰하여 자료화할 필요성이 있다. 또한 인위적인 훼손을 지속적으로 모니터링하고, 영양번식 및 종자번식의 과정을 자료화하여 다른 멸종위기종의 보호와 복원에 활용하는 중장기적인 연구가 필요하다.